新潟県工業技術総合研究所は、工業系の技術支援機関です。
| Topページ > 機械・金属関係 技術トピックス > XPS分析による銅の変色原因調査 |
一方、X線光電子分光(XPS)分析は、表面数nmにおける元素組成分析と化学結合状態(どんな化合物なのか)を調べることができる分析方法です。そのため、このXPS分析は銅表面の変色原因を調べるのに有効であると考えられます。
そこで、本研究では各種方法で表面を酸化させた銅板についてXPS分析を行い、どの様な皮膜が形成されているのかについて検討を行いました。
実験に供した試験片は、20×20×0.5mmのりん脱酸銅(C1220)です。これを20vol% H2SO4水溶液(液温30℃)に10分間浸漬して酸化皮膜を除去(未処理)後、恒温恒湿器を用いた湿式酸化および電気炉を用いた高温酸化を行いました。 恒温恒湿器では、試験片2枚を重ねて温度60℃、湿度90%RHにて144時間静置(湿式酸化60℃)しました。電気炉では200℃(高温酸化200℃)、300℃(高温酸化300℃)、400℃(高温酸化400 ℃)で10分間の加熱を行いました。
2.2 表面分析
上記の5試料について、X線光電子分光(XPS)分析装置(サーモフィッシャーサイエンティフィック(株)製K-Alpha)を用いて、Cu2p、CuLMMオージェ電子およびO1sのスペクトルを測定しました。これらの測定では、X線源は単色Al Kα線、照射径は400μmとし、中和銃を使用しました。また、スキャンは、パスエネルギー50eV、エネルギーステップ0.1eVとしました。
5試料の写真を図1に示します。湿式酸化60℃は斑のある橙色となっており、高温酸化200℃は全面が一様に橙色になっています。高温酸化300℃は金属光沢が抑えられたこげ茶色であり、高温酸化400℃は黒色で皮膜の一部が剝がれていました。 高温酸化による変色では、200℃付近でCu2Oが発生する1)ことから高温酸化200℃はCu2O皮膜の光の干渉による発色と考えられます。高温酸化300℃はこげ茶色、高温酸化400℃は黒色であることからCuOが生成していると推定できます。

3.2 XPS分析
3.2.1 Cu2pスペクトル
XPS分析では多くのCuに関するスペクトルが存在しますが、その中で定性や定量に用いられる主要なスペクトルは、Cu2pスペクトルです。そのCu2pスペクトルの測定結果を図2に示します。多くの元素は酸素と結合するとそのスペクトルは高エネルギー側へシフトし、結合する酸素の数が多くなるほどシフトの量が大きくなります。そのためこのシフト量からどの様な化学結合状態であるかを判断できます。
しかし、Cuでは、金属Cu、Cu2O、CuOのピーク位置は、932.6eV、932.7eV、933.1 eVと近い位置にあるため、933eV付近のピークでは、これらの化学状態の区別は困難です。ただしCu2OとCuOの区別についてはサテライトピークで判断します。未処理と高温酸化200℃では、943~948eV付近にCu2Oに由来するサテライトピークが確認され、湿式酸化60℃、高温酸化300℃、400℃では、940~945eV付近にCuOに由来するサテライトピークが確認されました。
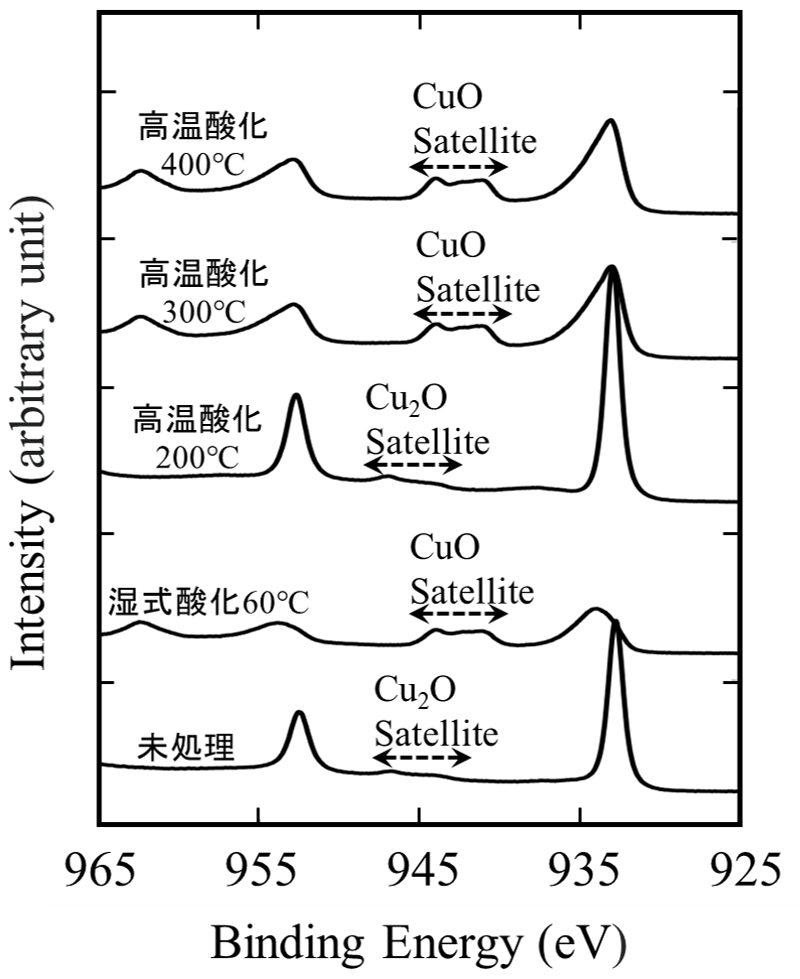
3.2.2 CuLMMオージェ電子スペクトル
図3のCuLMMオージェ電子スペクトルにおいて、未処理では、Cu(918.7eV)とCu2O(916.2eV)に由来するピークが出ており、高温酸化200℃では、Cu2Oに由来のピークのみ確認されました。また、湿式酸化60℃、高温酸化300℃、400℃では、CuO(917.6eV )に由来のピークが見られました。湿式酸化60℃と高温酸化200℃は、どちらも橙色に変色していますが、XPS分析によって、各々に異なる酸化膜が生成していることが確認できました。なお、CuLMMオージェ電子スペクトルの横軸は、運動エネルギー(940~900 eV)で示していますが、結合エネルギーに換算すると546.6~586.6eVとなります。
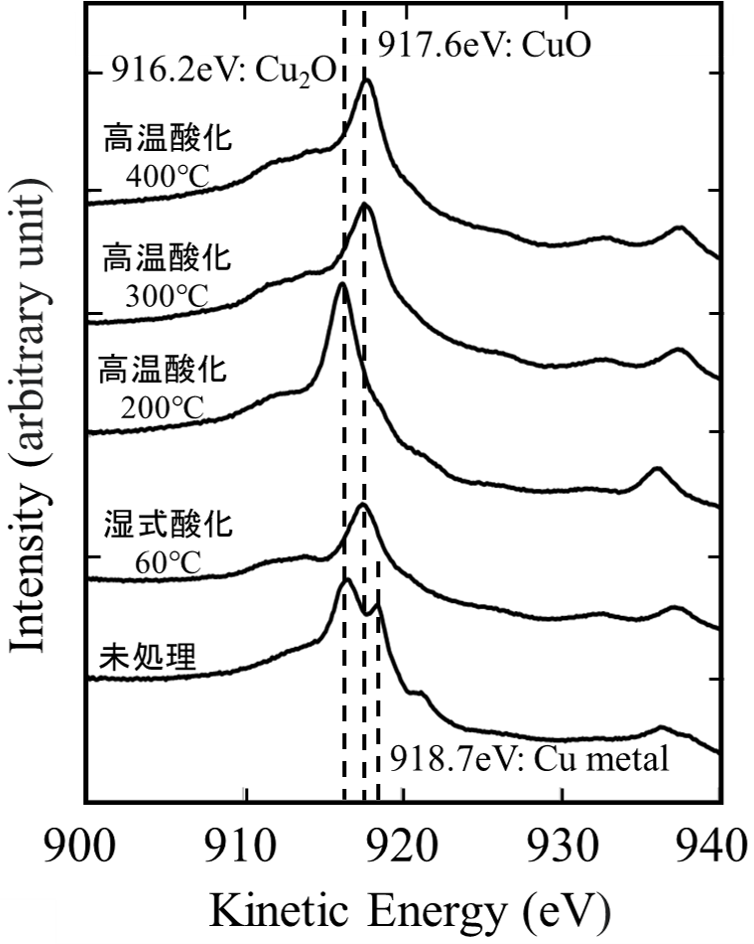
3.2.3 O1sスペクトル
図4のO1sスペクトルにおいて、未処理と高温酸化200℃はCu2O由来のピーク(530.7 eV)、湿式酸化60℃、高温酸化300℃、400℃はCuO由来のピーク(529.8eV)が確認されました。これらはCuLMMオージェ電子スペクトルの傾向と一致しており、高温酸化200℃以外の試料ではCu(OH)2由来のピーク(531.7eV)も確認された。また、湿式酸化60℃、高温酸化300℃、400℃において、ベースラインを引いて求めたCuOとCu(OH)2のピーク高さ比(CuOの高さを1とする)は、各々0.44、0.15、0.14です。このことから、3試料の生成物は同じですが、湿式酸化では高温酸化よりもCu(OH)2の生成量が多いことがわかりました。
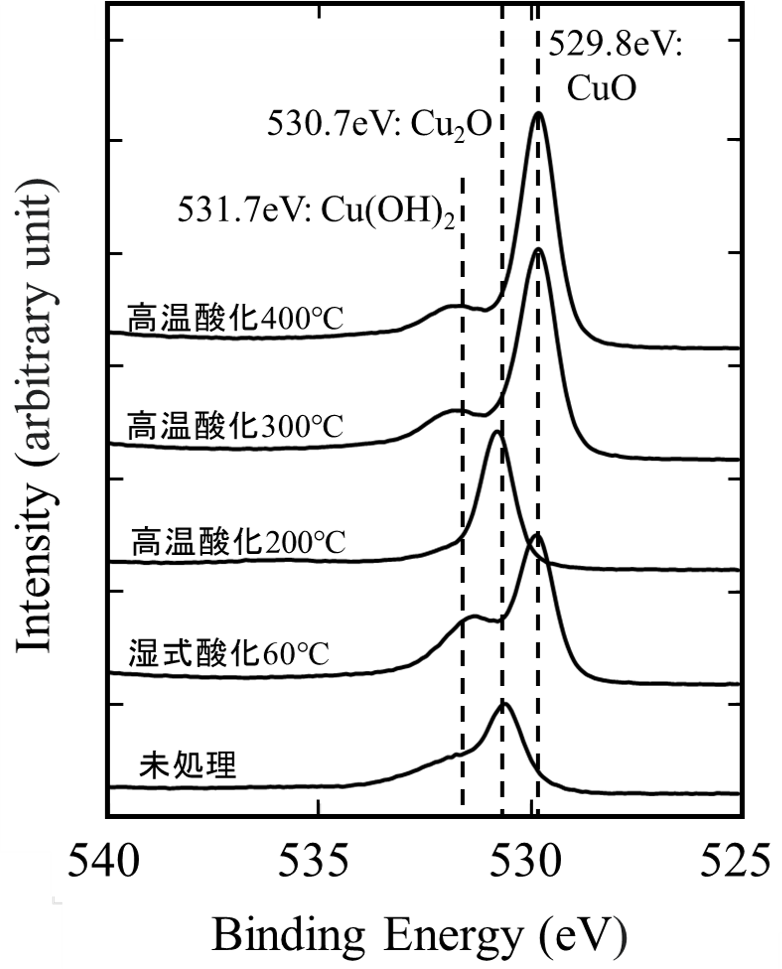
- 60℃の湿式酸化と300℃、400℃の高温酸化では、銅表面にCuOとCu(OH)2が存在し、200℃の高温酸化ではCu2Oのみが存在していることが確認できました。
- 60℃の湿式酸化と200℃の高温酸化では、どちらも橙色に変色しましたが、XPS分析によって皮膜構造の違いが確認できました。
- XPS分析でCu2p、CuLMMオージェ電子、O1sスペクトルを測定することにより銅表面の構造を明らかにすることができ、銅の変色原因調査に有効であることがわかりました。
2)S. Nakayama, T. Notoya, and T. Osakai, “A Mechanism for the Atmospheric Corrosion of Copper Determined by Voltammetry with a Strongly Alkaline Electrolyte”J. Electrochem. Soc., Vol.157, No.9, 2010, C289-C294.
|
問い合わせ:新潟県工業技術総合研究所 下越技術支援センター 諸橋 春夫 TEL:025-244-9168 FAX:025-241-5018 (令和4年3月28日) |